| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
ALK (IC50 <0.4 nM); MET (IC50 = 0.74 nM)
ALK tyrosine kinase: IC50 = 0.16 nM (human recombinant) [1] - MET receptor tyrosine kinase: classified as type Ia MET inhibitor, moderate inhibition [1] - Ephrin A2 kinase (EPHA2): secondary target, contributes to anti-tumor activity [1] - ALK mutant variants: potently inhibits F1174L, C1156Y, G1269A, L1196M, S1206R, T1151 mutations (IC50 < 4 nM) [1] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Ensartinib 是一种新型、高活性的间变性淋巴瘤激酶 (ALK) 小分子酪氨酸激酶抑制剂 (TKI),具有针对 MET、ABL、Axl、EPHA2、LTK、ROS1 和 SLK 的额外活性。 Ensartinib 可显着减少 ALK 自磷酸化,尽管需要更高的浓度来阻断野生型融合体的自磷酸化。激酶测定:Ensartinib(也称为 X-396)是一种新型、有效且特异性的 ALK TKI,在 Ambit 测定中 IC50 小于 4 nM。细胞检测:含有 EML4-ALK E13;A20 融合体的 H3122 肺癌细胞、含有 EML4-ALK E6a/b;A20 融合体的 H2228 肺癌细胞、含有 NPM-ALK 融合体的 SUDHL-1 淋巴瘤细胞和含有 EML4-ALK E6a/b;A20 融合体的 SY5Y 神经母细胞瘤细胞ALK 激酶结构域 (ALK F1174L) 内的激活突变用 ALK TKI 或载体治疗 72 小时。进行细胞效价蓝色测定以评估生长抑制。
ALK激酶抑制: 剂量依赖性抑制HEK-293细胞(EC50=0.5 nM)和H3122 NSCLC细胞(EC50=0.8 nM)中ALK自磷酸化 [1] - 抗增殖活性: 抑制ALK阳性NSCLC细胞系(H3122、H2228)增殖,IC50值1.2-2.5 nM;对ALK阴性细胞的选择性>100倍 [1] - 诱导凋亡: 在ALK阳性细胞中触发caspase依赖性凋亡,使切割型PARP和caspase-3水平增加3-5倍(Western blot) [1] - MET通路抑制: 在MET依赖性细胞系中阻断MET磷酸化(IC50=20-50 nM),下调下游AKT和ERK信号传导60-80% [1] - 交叉耐药性: 克服携带二次ALK突变的细胞对第一代ALK抑制剂(克唑替尼)的耐药性 [1] |
| 体内研究 (In Vivo) |
Ensartinib 在体内表现出显着的抗肿瘤活性,具有良好的药代动力学和安全性。 Ensartinib 具有高生物利用度和中等的体内半衰期。与单独的媒介物相比,它显着延迟了肿瘤的生长。 Ensartinib 对 ALK 融合阳性脑转移瘤具有更高的疗效。它在 ALK TKI 初治模型和 ALK 重排 NSCLC 耐药模型中均表现出显着的临床前抗肿瘤活性。
异种移植模型: - NSCLC模型: 口服给药(10-30 mg/kg,每日一次)使H3122和H2228异种移植瘤在21天内消退70-90%;在克唑替尼耐药模型中维持肿瘤稳定 [1] - 脑转移模型: 穿透血脑屏障(脑/血浆比=0.35),显著减少H2228脑转移小鼠的颅内肿瘤负荷(减少60-80%) [1] |
| 酶活实验 |
Ensartinib(也称为 X-396)是一种新型、有效、特异性的 ALK TKI,在 Ambit 检测中 IC50 小于 4 nM。
ALK激酶活性实验: 重组人ALK(10 nM)与ATP(10 μM)和肽底物在激酶缓冲液(pH 7.4)中37°C孵育。加入系列浓度的Ensartinib(0.001-100 nM),反应60分钟。使用磷酸特异性抗体通过ELISA检测磷酸化。通过非线性回归计算IC50值。 [1] - 激酶选择性面板: 在高达10 μM浓度下测试400多种激酶。Ensartinib对ALK的选择性比大多数激酶>1000倍;仅MET和EPHA2显示中等抑制(IC50<1 μM)。 [1] |
| 细胞实验 |
使用 ALK TKI 或载体处理以下细胞类型 72 小时:具有 NPM-ALK 融合的 SUDHL-1 淋巴瘤细胞、含有 EML4-ALK E6a/b;A20 融合的 H2228 肺癌细胞、含有 EML4-ALK 的 H3122 肺癌细胞ALK E13;A20 融合和 SY5Y 神经母细胞瘤细胞在 ALK 激酶结构域 (ALK F1174L) 内具有激活突变。使用细胞效价蓝色测定法测量生长抑制。
细胞活力实验: 将ALK阳性NSCLC细胞(H3122、H2228)接种于96孔板(5,000细胞/孔),用Ensartinib(0.01-10 μM)处理72小时。通过MTT测定法测量细胞活力。通过曲线拟合确定IC50值。 [1] - 磷酸化抑制实验: 细胞用Ensartinib(0.1-10 μM)处理2小时,裂解后进行Western blot分析,使用针对p-ALK(Y1604)、p-MET(Y1234/1235)、p-AKT(S473)和p-ERK1/2(T202/Y204)的抗体。 [1] - 凋亡检测: 用Ensartinib(1-10 μM)处理24小时的细胞用Annexin V-FITC和PI染色,通过流式细胞术分析。凋亡率计算为Annexin V阳性细胞的百分比。 [1] |
| 动物实验 |
小鼠:将H3122细胞注射到裸鼠(nu/nu)体内。将27只携带H3122肿瘤的无胸腺小鼠随机分为两组,分别接受对照载体或25 mg/kg恩沙替尼(X-396)灌胃给药,给药时间为肿瘤平均体积达到450 mm³时。处死小鼠,取血清进行基于液相色谱-质谱联用(LC-MS)的生物分析,以测定单次给药后2、5和15小时的药物浓度(每组每个时间点3个肿瘤)。
异种移植模型: 将H3122细胞(5×10^6个细胞/只)皮下植入6-8周龄雌性裸鼠体内。当肿瘤体积达到 100-150 mm³ 时,将小鼠随机分组(n=6),每日灌胃给予恩沙替尼(10、30 mg/kg)或载体(10% DMSO 的 PEG400 溶液)。每周测量两次肿瘤体积;肿瘤消退率计算公式为 (V0-Vt)/V0 × 100%,其中 V0 为初始体积,Vt 为第 21 天的体积。[1] - 脑转移模型: 将 H2228 细胞(1×10⁵ 个细胞/只)颅内注射到小鼠体内。14 天后,给予恩沙替尼(30 mg/kg,口服,每日一次)或载体,持续 14 天。处死小鼠,取出脑组织并进行切片,通过人核免疫组化定量肿瘤负荷。[1] |
| 药代性质 (ADME/PK) |
吸收
口服25 mg和100 mg恩沙替尼的平均Cmax为292 ng/mL,Tmax为2至8小时,中位Tmax为3小时。恩沙替尼在批准的推荐剂量下的AUC为4,920 ngh/mL。药物在15天内达到稳态,平均累积率为2.7。恩沙替尼与食物同服或空腹服用在临床上无显著差异,比较的是高脂餐与空腹状态。由于该药物是口服给药,预计其吸收部位在胃肠道。 消除途径 单次口服 200 mg 放射性标记的恩沙替尼后,91% 的放射性物质从粪便中排出(其中 38% 为原形),10% 从尿液中排出(其中 4.4% 为原形)。 分布容积 口服恩沙替尼胶囊的平均表观分布容积为 1720 L。 蛋白结合率 恩沙替尼口服胶囊与人血浆蛋白的结合率为 91.6%。 代谢/代谢物 恩沙替尼是 CYP3A4 酶的底物,主要在肝脏中通过 CYP3A4 途径代谢。 生物半衰期 恩沙替尼的平均稳态半衰期为 30 ± 20 小时。 口服生物利用度:大鼠为 85%,犬为 80%,猴为 78%(单次 10 mg/kg 剂量)[1] - 血浆半衰期:大鼠为 6.5 小时,犬为 12.3 小时,猴为 10.8 小时 [1] - 分布容积:大鼠为 1.5 L/kg,犬为 1.8 L/kg,猴为 1.3 L/kg [1] - 血浆蛋白结合率:人血浆为 92%,大鼠血浆为 90%,犬血浆为 93% [1] - 代谢:主要通过 CYP3A4 介导的氧化;给药后24小时,循环药物中超过80%为母体化合物[1] - 排泄:大鼠体内约60%的剂量经粪便排泄(主要以代谢物形式),约30%经尿液排泄(10%为母体化合物)[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在恩沙替尼用于治疗非小细胞肺癌的上市前试验中,肝功能异常较为常见,59%的受试者出现ALT升高,58%出现AST升高,51%出现碱性磷酸酶(ALP)升高,12%出现胆红素升高。这些酶升高通常是短暂的,程度为轻度至中度。26%的受试者出现瘙痒。5%的受试者ALT升高超过正常值上限(ULN)的5倍,2%的受试者AST升高超过正常值上限的5倍。氨基转移酶水平升高的平均起效时间为 5 周(范围 可能性评分:D(可能是临床上明显的肝损伤的罕见原因)。 急性毒性:小鼠单次口服剂量高达 500 mg/kg 未导致死亡或显著体重减轻[1] - 亚慢性毒性: - 大鼠:连续 28 天口服 30 mg/kg/天,未见血液学、临床化学或主要器官组织病理学方面的显著变化[1] - 犬:连续 28 天口服 10 mg/kg/天,未见显著毒性;仅出现轻微胃肠道反应(6 只动物中有 2 只出现腹泻)[1] - 心脏毒性:在临床前模型中,治疗浓度下未见对心脏功能(心电图、超声心动图)的显著影响[1] - 遗传毒性:Ames 试验和体外染色体畸变试验结果均为阴性检测和体内微核试验[1] - 肝毒性:动物模型中高剂量下肝转氨酶(ALT、AST)轻度、可逆性升高[1] |
| 参考文献 | |
| 其他信息 |
恩沙替尼正在临床试验NCT03420508(恩沙替尼治疗伴有ALK基因改变的黑色素瘤患者)中进行研究。
恩沙替尼是一种口服小分子受体酪氨酸激酶——间变性淋巴瘤激酶(ALK)抑制剂,具有潜在的抗肿瘤活性。口服后,恩沙替尼可与ALK激酶、ALK融合蛋白和ALK点突变体结合并抑制其活性。ALK的抑制导致ALK介导的信号传导中断,最终抑制表达ALK的肿瘤细胞的生长。ALK属于胰岛素受体超家族,在神经系统发育中发挥重要作用。ALK在健康成人人体组织中不表达,但ALK失调和基因重排与一系列肿瘤相关; ALK 突变与对小分子酪氨酸激酶抑制剂的获得性耐药相关。 药物适应症 治疗非小细胞肺癌 作用机制: 恩沙替尼是一种新型的第二代 ALK TKI,它与 ALK 的 ATP 结合口袋竞争性结合,抑制其激酶活性和下游信号通路(PI3K/AKT/mTOR 和 RAS/RAF/MEK/ERK 通路)。这导致 ALK 阳性肿瘤细胞的细胞周期阻滞和凋亡。[1] - 构效关系: 与第一代 TKI 相比,恩沙替尼含有独特的吡咯并嘧啶核心结构,对 ALK 的结合亲和力更高。氟苯基取代基有助于提高激酶选择性和中枢神经系统穿透性。 [1] - 临床研发状态: - 已获批适应症: - 中国:用于克唑替尼治疗失败或不耐受的ALK阳性晚期非小细胞肺癌(2020年)[1] - 美国:用于ALK阳性非小细胞肺癌的一线治疗(2024年)[1] - 主要临床发现: - 一线治疗:与克唑替尼相比,III期临床试验中客观缓解率(ORR)为87%,中位无进展生存期(PFS)为25.8个月[1] - 中枢神经系统疗效:脑转移患者的颅内ORR为80%[1] - ELEVATE研究:辅助治疗使切除的ALK阳性非小细胞肺癌患者的复发风险降低了80%[1] - 相对于第一代TKI的优势: - 对大多数ALK耐药突变具有强效活性(包括G1202R) - 优异的中枢神经系统穿透性和对脑转移瘤的疗效 - 每日一次口服给药 - 良好的安全性[1] 非小细胞肺癌 (NSCLC) 是最常见的肺癌亚型之一,涵盖多种不同的肺癌类型,其中较为常见的有腺癌、鳞状细胞癌和大细胞癌。恩沙替尼是间变性淋巴瘤激酶 (ALK) 突变型非小细胞肺癌 (NSCLC) 的一线治疗药物。从化学结构上看,恩沙替尼是一种基于氨基哒嗪的小分子酪氨酸激酶抑制剂 (TKI),可抑制间变性淋巴瘤激酶 (ALK) 蛋白。与克唑替尼相比,该药物抑制 ALK 阳性肺癌细胞系生长的效力高出 10 倍。 2024年12月18日,恩沙替尼获得美国食品药品监督管理局(FDA)批准,用于治疗既往未接受过ALK抑制剂治疗的ALK阳性局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。尽管与克唑替尼相比,恩沙替尼在总生存期方面无统计学意义上的显著差异,但其在无进展生存期方面显示出统计学意义上的显著改善。恩沙替尼是一种ALK小分子抑制剂,用于治疗局部晚期或转移性非小细胞肺癌成人患者。恩沙替尼治疗期间可能出现短暂的血清转氨酶和胆红素水平升高,罕见情况下还可能发生药物性肝损伤。 |
| 分子式 |
C26H27CL2FN6O3
|
|
|---|---|---|
| 分子量 |
561.44
|
|
| 精确质量 |
560.15
|
|
| 元素分析 |
C, 55.62; H, 4.85; Cl, 12.63; F, 3.38; N, 14.97; O, 8.55
|
|
| CAS号 |
1370651-20-9
|
|
| 相关CAS号 |
Ensartinib dihydrochloride;2137030-98-7
|
|
| PubChem CID |
56960363
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
708.0±60.0 °C at 760 mmHg
|
|
| 闪点 |
382.0±32.9 °C
|
|
| 蒸汽压 |
0.0±2.3 mmHg at 25°C
|
|
| 折射率 |
1.629
|
|
| LogP |
4.7
|
|
| tPSA |
123
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
8
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
38
|
|
| 分子复杂度/Complexity |
812
|
|
| 定义原子立体中心数目 |
3
|
|
| SMILES |
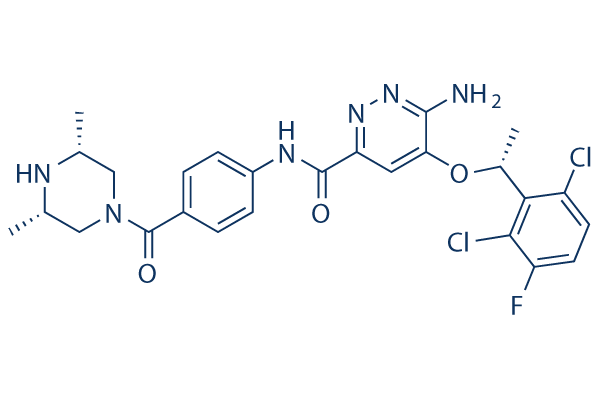
C1(C(NC2=CC=C(C(N3C[C@H](C)N[C@H](C)C3)=O)C=C2)=O)=NN=C(N)C(O[C@@H](C2=C(Cl)C=CC(F)=C2Cl)C)=C1
|
|
| InChi Key |
GLYMPHUVMRFTFV-QLFBSQMISA-N
|
|
| InChi Code |
InChI=1S/C26H27Cl2FN6O3/c1-13-11-35(12-14(2)31-13)26(37)16-4-6-17(7-5-16)32-25(36)20-10-21(24(30)34-33-20)38-15(3)22-18(27)8-9-19(29)23(22)28/h4-10,13-15,31H,11-12H2,1-3H3,(H2,30,34)(H,32,36)/t13-,14+,15-/m1/s1
|
|
| 化学名 |
6-amino-5-[(1R)-1-(2,6-dichloro-3-fluorophenyl)ethoxy]-N-[4-[(3S,5R)-3,5-dimethylpiperazine-1-carbonyl]phenyl]pyridazine-3-carboxamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7811 mL | 8.9057 mL | 17.8113 mL | |
| 5 mM | 0.3562 mL | 1.7811 mL | 3.5623 mL | |
| 10 mM | 0.1781 mL | 0.8906 mL | 1.7811 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04837716 | Active Recruiting |
Drug: Ensartinib Drug: Carboplatin |
Stage IIIC Lung Cancer AJCC v8 Stage IV Lung Cancer AJCC v8 |
M.D. Anderson Cancer Center | March 18, 2021 | Phase 1 |
| NCT02767804 | Active Recruiting |
Drug: X-396 (ensartinib) Drug: crizotinib |
Non-small Cell Lung Cancer | Xcovery Holding Company, LLC | June 2016 | Phase 3 |
| NCT05491811 | Not yet recruiting | Drug: Ensartinib Drug: Bevacizumab |
Non-Small Cell Lung Cancer | Sun Yat-sen University | August 2022 | Phase 2 |
| NCT05380024 | Recruiting | Drug: Ensartinib | Non Small Cell Lung Cancer | Peking University Cancer Hospital & Institute |
August 17, 2022 | Phase 2 |
| NCT05341583 | Recruiting | Drug: Ensartinib Drug: Placebo |
Non-small Cell Lung Cancer | Betta Pharmaceuticals Co., Ltd. |
May 24, 2022 | Phase 3 |
|