| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |

| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服后,消旋米那普仑的绝对生物利用度约为 85-90%。口服给药后 2-4 小时内即可达到最大血药浓度,并在 36-48 小时内达到稳态血药浓度。相比之下,左旋米那普仑的相对生物利用度已证实为 92%。左旋米那普仑的达峰时间 (Tmax) 中位数为口服给药后 6-8 小时。每日服用 120 mg 左旋米那普仑后,平均 Cmax 值为 341 ng/mL,平均稳态 AUC 值为 5196 ng·h/mL。通常情况下,与食物同服消旋米那普仑或左旋米那普仑不会影响药物的口服生物利用度。 左旋米那普仑及其代谢物主要经肾脏排泄。口服14C-左旋米那普仑溶液后,约58%的剂量以原形左旋米那普仑的形式经尿液排出。N-去乙基左旋米那普仑是尿液中排泄的主要代谢物,约占剂量的18%。尿液中排泄的其他可识别代谢物包括左旋米那普仑葡糖苷酸(4%)、去乙基左旋米那普仑葡糖苷酸(3%)、对羟基左旋米那普仑葡糖苷酸(1%)和对羟基左旋米那普仑(1%)。 健康受试者单次静脉注射消旋米那普仑后,记录的平均分布容积约为400升。而左旋米那普仑分布广泛,表观分布容积为387-473升。 米那普仑的总血浆清除率约为40升/小时。 代谢/代谢物 已确定左旋米那普仑经去乙基化和羟基化分别生成去乙基左旋米那普仑和对羟基左旋米那普仑。两种氧化代谢产物均进一步与葡萄糖醛酸苷结合,形成结合物米那普仑氨甲酰-O-葡萄糖醛酸苷。脱乙基化主要由CYP3A4催化,CYP2C8、2C19、2D6和2J2的贡献较小。此外,普遍认为米那普仑的对映异构体在体内不会相互转化。 生物半衰期 已记录的消旋米那普仑的末端消除半衰期约为6-8小时,而d-米那普仑的消除半衰期为8-10小时,比l-对映异构体的4-6小时更长。或者,专门针对左旋米那普仑制剂测定的末端消除半衰期约为12小时。 |
|---|---|
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期影响
◉ 哺乳期用药概述 母乳中米那普仑的含量很低,预计不会对母乳喂养的婴儿造成任何不良影响。但是,在获得更多数据之前,哺乳期妇女应谨慎使用米那普仑,尤其是在哺乳新生儿或早产儿时。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 据生产商报告,溢乳是米那普仑的副作用之一。一名正在接受抑郁症治疗的女性故意口服过量950毫克米那普仑。从过量服用后的第5天到第15天,该患者注意到左侧乳房有乳汁流出。溢乳症状无需治疗即可自行缓解。 一项针对法国药物警戒中心报告的高泌乳素血症及其症状(例如男性乳房发育症)病例的研究发现,与其他药物相比,米那普仑并未增加引起高泌乳素血症的风险。 一项观察性研究调查了2859名在孕前两年服用抗抑郁药的女性的结局。与孕期未服用抗抑郁药的女性相比,孕期三个阶段均服用抗抑郁药的母亲出院时母乳喂养的可能性降低了37%。仅在孕晚期服用抗抑郁药的母亲出院时母乳喂养的可能性降低了75%。仅在孕早期和孕中期服用抗抑郁药的母亲出院时母乳喂养的可能性并未降低。未具体说明母亲们使用的抗抑郁药。 一项回顾性队列研究分析了2001年至2008年间医院的电子病历,比较了妊娠晚期服用过抗抑郁药的女性(n = 575)、患有精神疾病但未服用抗抑郁药的女性(n = 1552)以及未被诊断出患有精神疾病的母亲(n = 30,535)。结果显示,服用过抗抑郁药的女性出院时母乳喂养的可能性比未被诊断出患有精神疾病的女性低37%,但与未被治疗的患有精神疾病的母亲相比,母乳喂养的可能性并无显著差异。所有母亲均未服用米那普仑。 一项针对1999年至2008年间80,882对挪威母婴的研究显示,392名女性报告产后开始服用抗抑郁药,另有201名女性报告从孕期开始服用抗抑郁药。与未接触抗抑郁药的对照组相比,孕晚期服用抗抑郁药与母乳喂养启动率降低7%相关,但对母乳喂养持续时间或纯母乳喂养率无影响。与未接触抗抑郁药的对照组相比,产后开始或重新开始服用抗抑郁药与6个月时以母乳为主的喂养率降低63%,任何形式的母乳喂养率降低51%,以及突然停止母乳喂养的风险增加2.6倍相关。未提及具体抗抑郁药。 蛋白质结合 消旋米那普仑的蛋白质结合率为13%。相反,左旋米那普仑在10至1000 ng/mL的浓度范围内,血浆蛋白结合率为22%。 |
| 参考文献 | |
| 其他信息 |
药效学
在用于治疗纤维肌痛时,一项双盲、安慰剂对照和阳性对照平行研究测量了米那普仑对患者QTcF间期的影响。该研究纳入88名健康受试者,使用纤维肌痛推荐治疗剂量的3至6倍(600 mg/天)。经基线和安慰剂校正后,QTcF间期的最大平均变化为8毫秒——这种增加通常被认为不具有临床意义。相反,在用于治疗重度抑郁症(MDD)时,非临床研究表明,左旋米那普仑与去甲肾上腺素(NE)和5-羟色胺(5-HT)转运体具有高亲和力结合(在人体转运体上的Ki值分别为71-91 nM和11 nM)。左旋米那普仑在体外和体内均能抑制NE和5-HT的摄取;左米那普仑对去甲肾上腺素(NE)的再摄取抑制作用约为5-羟色胺(5-HT)的两倍。左米那普仑不直接影响多巴胺或其他神经递质的摄取。体外实验表明,左米那普仑对血清素能受体(5-HT1-7)、α-和β-肾上腺素能受体、毒蕈碱受体(M1-5)、组胺受体(H1-4)、多巴胺受体(D1-5)、阿片受体、苯二氮卓受体和γ-氨基丁酸(GABA)受体均无显著亲和力。左米那普仑对Ca++、K+、Na+和Cl-通道也无显著亲和力,且不抑制人单胺氧化酶(MAO-A和MAO-B)或乙酰胆碱酯酶的活性。此外,在用左米那普仑治疗重度抑郁症(MDD)的心电图研究中,虽然未观察到QTcF间期(QTcF=QT/RR0.33)的临床显著变化,但该药物似乎可导致心率和血压升高。特别是,每日120毫克左米那普仑的最大治疗剂量似乎可使心率较安慰剂组平均升高20.2次/分,收缩压和舒张压较安慰剂组平均升高3.8至7.2 mmHg和6.1至8.1 mmHg。或者,每天服用 300 毫克的超治疗剂量,可使心率与安慰剂相比平均最大差异达到 22.1 次/分钟,收缩压和舒张压与安慰剂相比平均差异分别为 5.4 至 7.9 毫米汞柱和 7.9 至 10.6 毫米汞柱。 |
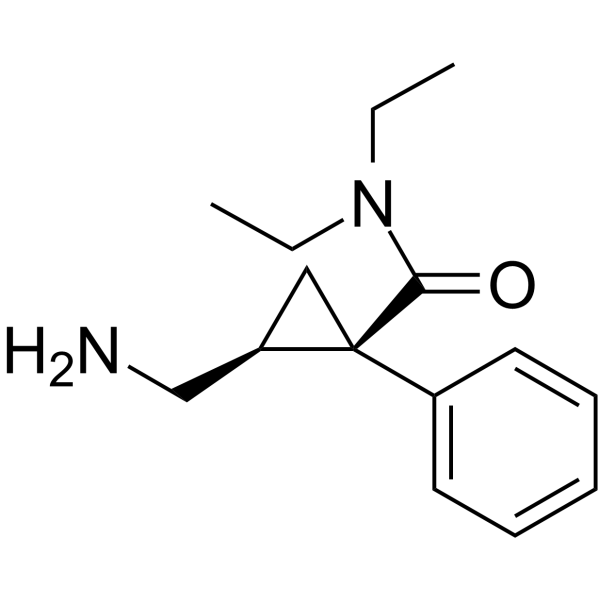
| 分子式 |
C15H22N2O
|
|---|---|
| 分子量 |
246.34798
|
| 精确质量 |
246.173
|
| CAS号 |
92623-85-3
|
| 相关CAS号 |
Milnacipran hydrochloride;101152-94-7;Milnacipran ((1S-cis) hydrochloride);175131-60-9;Dextromilnacipran;96847-55-1;Milnacipran-d10 hydrochloride;1217774-40-7
|
| PubChem CID |
65833
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
393.0±21.0 °C at 760 mmHg
|
| 熔点 |
179°C
|
| 闪点 |
191.5±22.1 °C
|
| 蒸汽压 |
0.0±0.9 mmHg at 25°C
|
| 折射率 |
1.554
|
| LogP |
1.23
|
| tPSA |
46.33
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
18
|
| 分子复杂度/Complexity |
295
|
| 定义原子立体中心数目 |
2
|
| SMILES |
C([C@@]1(C[C@@H]1CN)C1C=CC=CC=1)(=O)N(CC)CC
|
| InChi Key |
GJJFMKBJSRMPLA-HIFRSBDPSA-N
|
| InChi Code |
InChI=1S/C15H22N2O/c1-3-17(4-2)14(18)15(10-13(15)11-16)12-8-6-5-7-9-12/h5-9,13H,3-4,10-11,16H2,1-2H3/t13-,15+/m1/s1
|
| 化学名 |
(1R,2S)-2-(aminomethyl)-N,N-diethyl-1-phenylcyclopropane-1-carboxamide
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 4.0593 mL | 20.2963 mL | 40.5927 mL | |
| 5 mM | 0.8119 mL | 4.0593 mL | 8.1185 mL | |
| 10 mM | 0.4059 mL | 2.0296 mL | 4.0593 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT02783430
Conditions:DepressionLink: https://clinicaltrials.gov/ct2/show/NCT01829243
Conditions:Fibromyalgia|NeurocognitionLink: https://clinicaltrials.gov/ct2/show/NCT01393522
Conditions:Chronic Migraine
Title:Effect of Milnacipran / Gabapentin in Fibromyalgia
Status:Unknown status
updateDate:2022-05-20
Ctid:NCT05384210
Link: https://clinicaltrials.gov/ct2/show/NCT05384210
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01288937
Conditions:Idiopathic Peripheral NeuropathyLink: https://clinicaltrials.gov/ct2/show/NCT01337700
Conditions:Autism Spectrum Disorder|Asperger Syndrome|Aspergers SyndromeLink: https://clinicaltrials.gov/ct2/show/NCT01125423
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01234675
Conditions:Sleep Disorders|Fibromyalgia|SleepLink: https://clinicaltrials.gov/ct2/show/NCT01328002
Conditions:Primary FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01914042
Conditions:Neuropathic PainLink: https://clinicaltrials.gov/ct2/show/NCT01304589
Conditions:Vestibulodynia|VulvodyniaLink: https://clinicaltrials.gov/ct2/show/NCT01225991
Conditions:Rheumatoid ArthritisLink: https://clinicaltrials.gov/ct2/show/NCT01173055
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01471379
Conditions:Irritable Bowel SyndromeLink: https://clinicaltrials.gov/ct2/show/NCT01108731
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01359826
Conditions:Systemic Lupus Erythematosus|Widespread Pain|FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01510457
Conditions:Knee Osteoarthritis|Degenerative Joint Disease|Chronic PainLink: https://clinicaltrials.gov/ct2/show/NCT01207453
Conditions:Arthritis, RheumatoidLink: https://clinicaltrials.gov/ct2/show/NCT01294059
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01777581
Conditions:Radicular Pain Related to Lumbosacral Disc DiseaseLink: https://clinicaltrials.gov/ct2/show/NCT01747044
Conditions:FibromylagiaLink: https://clinicaltrials.gov/ct2/show/NCT01225068
Conditions:Low Back PainLink: https://clinicaltrials.gov/ct2/show/NCT01331109
Conditions:Primary FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT00757679
Conditions:Fibromyalgia SyndromeLink: https://clinicaltrials.gov/ct2/show/NCT00436033
Conditions:Fibromyalgia SyndromeLink: https://clinicaltrials.gov/ct2/show/NCT00757731
Conditions:Fibromyalgia SyndromeLink: https://clinicaltrials.gov/ct2/show/NCT01289236
Conditions:Chronic Shoulder PainLink: https://clinicaltrials.gov/ct2/show/NCT01077375
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01014585
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT01329406
Conditions:OsteoarthritisLink: https://clinicaltrials.gov/ct2/show/NCT01319825
Conditions:Migraine With Aura|Migraine Without Aura|Chronic MigraineLink: https://clinicaltrials.gov/ct2/show/NCT00793520
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT00314249
Conditions:FibromyalgiaLink: https://clinicaltrials.gov/ct2/show/NCT00606203
Conditions:Ischemic Stroke|DepressionLink: https://clinicaltrials.gov/ct2/show/NCT00225511
Conditions:Depression