| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |

| 靶点 |
Topoisomerase I 2.2 μM (IC50)
|
|---|---|
| 体外研究 (In Vitro) |
Exatecan 的 IC50 为 0.975 μg/mL,使其成为拓扑异构酶 I 的强抑制剂。exatecan 甲磺酸盐 (DX- 8951f)[1]。 exatecan mesylate (DX-8951f) 对 PC-6 和 PC-6/SN2-5 细胞的细胞毒作用通过平均 GI50 值分别为 0.186 和 0.395 ng/mL 得到证实。在 PC-6 和 PC-6/SN2-5 细胞中,exatecan mesylate (34 nM) 可稳定 DNA-TopoI 复合物 [3]。
|
| 体内研究 (In Vivo) |
在具有肿瘤细胞但无毒性死亡的小鼠模型中,甲磺酸exatecan(DX-8951f,3.325-50 mg/kg,静脉注射)显示出抗肿瘤功效[1]。在 MIA-PaCa-2 早期模型和 BxPC-3 早期模型中,exatecan Mesylate(15、25 mg/kg,静脉注射)显着抑制 MIA-PaCa 和 BxPC-3 原发肿瘤的生长。在BxPC-3晚期癌症模型中,甲磺酸exatecan(15、25mg/kg,静脉注射)完全根除肺转移并显着减少BxPC-3淋巴转移[2]。
|
| 酶活实验 |
细胞裂解和蛋白质印迹:[3]
使用SDS缓冲液(10 mM HEPES、2 mM正钒酸盐、10 mM NaF、10 mM焦磷酸盐、1 mM PMSF、10µg/mL亮肽、10%2-巯基乙醇、10%甘油、8%SDS、42 mM Tris-HCl、0.002%溴酚蓝,pH 7.4)裂解细胞(5×10⁶)。通过7.5%聚丙烯酰胺凝胶电泳分离全细胞裂解物中的蛋白质,并将其转移到硝化纤维膜上。用抗Topo I人抗体探测膜,然后用辣根过氧化物酶偶联蛋白A孵育。使用ECL试剂观察Topo I特异性条带。 核提取物制备:[3] 对于核提取物,用冰冷的缓冲液(2 mM K₂HPO₄,5 mM氯化镁,150 mM NaCl、1 mM EGTA、0.1 mM二硫苏糖醇),重新悬浮在含有0.35%Triton-X100和PMSF的缓冲液中,在冰上孵育10分钟。裂解物离心,所得沉淀在4°C下与含有0.35 M NaCl的缓冲液进一步孵育1小时。离心(18000×g,10分钟)后,使用Bradford法和蛋白质测定试剂盒测定上清液(核提取物)的蛋白质浓度。然后用抗Topo I抗体对等量的核蛋白进行蛋白质印迹分析。 |
| 细胞实验 |
生长抑制试验(MTT法):[1]
使用MTT法在96孔平底微孔板中评估细胞生长抑制。将细胞(500-20000/孔)接种在150μL培养基中,预孵育24小时(P388、CCRF-CEM和K562细胞为4小时)。然后加入试验化合物,包括甲磺酸Exatecan(150μL培养基/孔)或单独培养基(对照),然后孵育3天。处理后,向每个孔中加入20μL MTT溶液(PBS中5mg/mL),并将平板孵育4小时。将平板在800×g下离心5分钟,去除上清液,将甲氮晶体溶解在150μL DMSO中。使用微孔板读数器(3550型)在540nm处测量吸光度。 |
| 动物实验 |
实验设计和治疗方案[2]
早期模型(植入后3周) 动物分组:将原位植入BxPC-3-GFP或MIA-PaCa-2-GFP肿瘤的小鼠在植入后3周随机分为5组(每组n=5)。 第1组:未治疗对照组。 第2组和第3组:分别接受甲磺酸依沙替康治疗(剂量分别为25和15 mg/kg/次)。 第4组和第5组:分别接受吉西他滨治疗(剂量分别为300和150 mg/kg/次)。 晚期模型(植入后6周) 动物分组:将携带BxPC-3-GFP肿瘤的小鼠在植入后6周随机分为3组(每组n=20)。 第1组:未治疗对照组。 第2组:接受甲磺酸依沙替康治疗(25 mg/kg/次)。 第3组:接受吉西他滨治疗(300 mg/kg/次)。 给药方案 药物每周给药一次,持续3周,然后停药2周,再继续给药3周。 监测与分析 每周测量指标:原发肿瘤大小(计算公式为a × b² × 0.5,其中a为肿瘤较大直径,b为肿瘤较小直径)和体重。 终止:实验结束后处死小鼠,记录最终肿瘤重量和GFP成像结果(原发肿瘤和转移灶)。 |
| 参考文献 |
|
| 其他信息 |
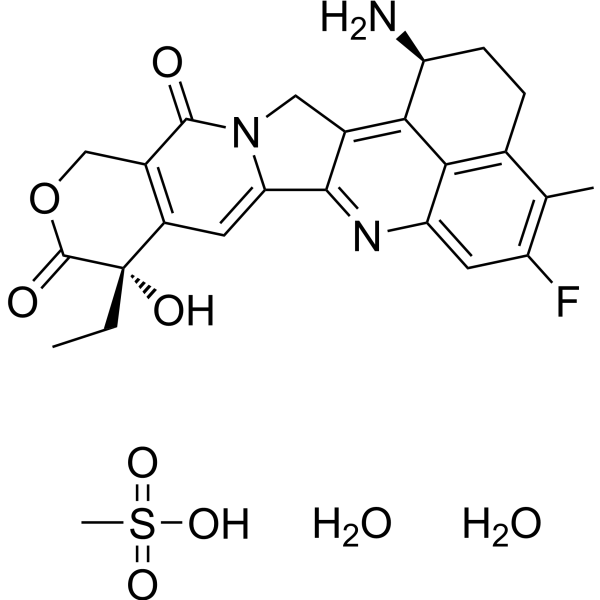
依沙替康甲磺酸盐水合物是一种吡喃并吲哚喹啉类化合物。
依沙替康甲磺酸盐是喜树碱的半合成水溶性衍生物,具有抗肿瘤活性。依沙替康甲磺酸盐通过稳定拓扑异构酶I与DNA之间的可裂解复合物并抑制DNA断裂的重新连接来抑制拓扑异构酶I的活性,从而抑制DNA复制并诱导细胞凋亡。该药物无需酶活化,且比喜树碱和其他喜树碱类似物具有更高的效力。 (NCI04) 依沙替康是一种吡喃并吲哚喹啉类化合物。 依沙替康已用于多种癌症的治疗试验,包括肉瘤、白血病、淋巴瘤、肺癌和肝癌等。 喜树碱的半合成衍生物CPT-11对淋巴瘤、肺癌、结直肠癌、胃癌、卵巢癌和宫颈癌均表现出强效的抗肿瘤活性。CPT-11是一种前药,在体内经羧酸酯酶等酶的作用转化为活性代谢物SN-38。我们合成了一种水溶性非前药形式的喜树碱类似物DX-8951f。该化合物对32种恶性细胞系均表现出较高的体外活性,并具有显著的拓扑异构酶I抑制作用。 DX-8951f 的抗增殖活性(以平均 GI50 值表示)分别比 SN-38 和 SK&F 10486-A(拓扑替康)高约 6 倍和 28 倍。这三种喜树碱衍生物在 32 种细胞系中表现出相似的差异反应模式,即它们的体外细胞毒性谱几乎相同。对人胃腺癌 SC-6 异种移植瘤,以 4 天为间隔静脉注射三次 DX-8951f 的抗肿瘤活性优于 CPT-11 或 SK&F 10486-A。此外,它还能克服 P-糖蛋白介导的多药耐药性。这些数据表明,DX-8951f 具有很高的抗肿瘤活性,是一种潜在的治疗药物。[1] 我们在胰腺癌原位转移小鼠模型中测定了喜树碱类似物 DX-8951f 的抗肿瘤和抗转移疗效。DX-8951f 在该模型中对两种人胰腺癌细胞系均显示出疗效。这些细胞系经绿色荧光蛋白转导,从而能够在体内高分辨率地观察肿瘤和转移灶的生长。DX-8951f 的研究包括早期和晚期癌症模型。在早期模型中,使用人胰腺癌细胞系 MIA-PaCa-2 和 BxPC-3,当原位原发肿瘤直径约为 7 mm 时开始治疗。DX-8951f 对 MIA-PaCa-2 和 BxPC-3 均具有显著疗效。相比之下,胰腺癌的标准治疗药物2',2'-二氟脱氧胞苷(吉西他滨)对MIA-PaCa-2细胞系疗效不佳。尽管吉西他滨对BxPC-3原发肿瘤的生长有显著抑制作用,但对转移灶无效。在BxPC-3晚期疾病模型中,当原位原发肿瘤直径达到13 mm时开始治疗。DX-8951f对BxPC-3原发肿瘤呈剂量依赖性显著抑制作用。DX-8951f在晚期模型中也表现出抗转移活性,显著降低了淋巴结转移的发生率,并消除了肺转移。相比之下,吉西他滨对原发肿瘤的抑制作用仅为中等,且在晚期模型中对原发和转移灶均无效。因此,DX-8951f 对这种极难治疗的疾病的原发性和转移性生长均表现出极高的疗效,并且其疗效显著高于胰腺癌的标准治疗药物吉西他滨。因此,DX-8951f 具有重要的临床应用前景,并且比目前使用的喜树碱类似物 CPT-11 具有更多优势,后者需要代谢活化且具有毒性。[2] 我们此前报道过,新型水溶性喜树碱类似物 DX-8951f 可显著抑制多种人类和小鼠肿瘤在体外和体内的生长。DX-8951f 的抗肿瘤作用和拓扑异构酶 I 抑制活性均强于其他现有的喜树碱类似物。本研究采用逐步筛选法,从人燕麦癌细胞系PC-6中分离得到SN-38耐药细胞系PC-6/SN2-5,并探讨了该细胞系的耐药机制,比较了喜树碱类似物对该细胞系的抗肿瘤活性。PC-6/SN2-5细胞对SN-38(耐药倍数32倍)和SK&F 104864(拓扑替康;耐药倍数14倍)的耐药性显著,但对CPT-11(耐药倍数3倍)和DX-8951f(耐药倍数2倍)的耐药性较低。亲代细胞的拓扑异构酶I蛋白水平和拓扑异构酶I活性与耐药细胞相似。通过流式细胞术或高效液相色谱法测定细胞内药物浓度,证实PC-6/SN2-5细胞中SN-38和拓扑替康的细胞内积累显著降低,而DX-8951f的细胞内积累仅略有降低。此外,DX-8951f能够稳定完整PC-6/SN2-5细胞及其亲代细胞中可裂解复合物的形成,而SN-38和拓扑替康在耐药细胞中则没有这种作用。我们的数据表明,PC-6/SN2-5细胞可能通过降低细胞内药物积累而获得对喜树碱类似物的耐药性,而DX-8951f可能具有克服喜树碱类化合物诱导的这种耐药机制的潜力。[3] |
| 分子式 |
C24H22FN3O4S.CH4O3S.2H2O
|
|---|---|
| 分子量 |
567.5838
|
| 精确质量 |
567.169
|
| CAS号 |
197720-53-9
|
| 相关CAS号 |
Exatecan;171335-80-1;Exatecan mesylate;169869-90-3;Exatecan-d5 mesylate;2819276-88-3;Dxd;1599440-33-1;Dxd-d5;Deruxtecan;1599440-13-7;Deruxtecan-d6;2760715-89-5;(1S,9R)-Exatecan mesylate;2938875-54-6;(1R,9R)-Exatecan mesylate;(1R)-Deruxtecan;2270986-87-1
|
| PubChem CID |
151114
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| 蒸汽压 |
2.47E-28mmHg at 25°C
|
| LogP |
3.629
|
| tPSA |
188.65
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
12
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
39
|
| 分子复杂度/Complexity |
1040
|
| 定义原子立体中心数目 |
2
|
| SMILES |
O.O.CS(=O)(O)=O.CC[C@]1(C(=O)OCC2C(N3CC4=C5[C@@H](N)CCC6=C5C(N=C4C3=CC1=2)=CC(=C6C)F)=O)O
|
| InChi Key |
FXQZOHBMBQTBMJ-MWPGLPCQSA-N
|
| InChi Code |
InChI=1S/C24H22FN3O4.CH4O3S.2H2O/c1-3-24(31)14-6-18-21-12(8-28(18)22(29)13(14)9-32-23(24)30)19-16(26)5-4-11-10(2)15(25)7-17(27-21)20(11)19;1-5(2,3)4;;/h6-7,16,31H,3-5,8-9,26H2,1-2H3;1H3,(H,2,3,4);2*1H2/t16-,24-;;;/m0.../s1
|
| 化学名 |
(10S,23S)-23-amino-10-ethyl-18-fluoro-10-hydroxy-19-methyl-8-oxa-4,15-diazahexacyclo[14.7.1.02,14.04,13.06,11.020,24]tetracosa-1,6(11),12,14,16,18,20(24)-heptaene-5,9-dione;methanesulfonic acid;dihydrate
|
| 别名 |
Exatecan mesilate hydrate; 197720-53-9; Exatecan mesylate hydrate; Exatecan mesylate [USAN]; exatecan mesylate dihydrate; DX-8951f; Exatecan methanesulfonate dihydrate; Exatecan mesilate dihydrate;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7619 mL | 8.8093 mL | 17.6187 mL | |
| 5 mM | 0.3524 mL | 1.7619 mL | 3.5237 mL | |
| 10 mM | 0.1762 mL | 0.8809 mL | 1.7619 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。