| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| 5g |
|
||
| 10g |
|
||
| Other Sizes |
|
| 靶点 |
17α-hydroxylase (IC50 = 2.5 nM); 17,20-lyase (IC50 = 15 nM)
Abiraterone primarily targets steroidogenic enzymes involved in androgen synthesis: - Cytochrome P450 17A1 (CYP17A1) (17α-hydroxylase/C17,20-lyase): Inhibits both subactivities with a Ki value of 15 ± 2 nM (for C17,20-lyase) and IC50 of 22 ± 3 nM (for 17α-hydroxylase) using human recombinant CYP17A1 [2, 3, 4] - 3β-Hydroxysteroid dehydrogenase (3β-HSD): Inhibits human 3β-HSD type 1 and 2 with an IC50 of 2.5 ± 0.4 μM (using pregnenolone as substrate) [4] - It has minimal affinity for the androgen receptor (AR): Ki > 10 μM for wild-type AR and mutant AR (e.g., AR-V7), showing no direct AR antagonism [2] |
|---|---|
| 体外研究 (In Vitro) |
已经确定,阿比特龙剂量≥5 μM 可显着限制 AR 阳性前列腺癌细胞系 LNCaP 和 VCaP 的增殖[2]。对于 17,20-裂解酶和 17α-羟化酶,阿比特龙的 IC50 值为 15 nM 和 2.5 nM(CYP17 是一种双功能酶,具有 17α-羟化酶和 17,20-裂解酶活性)。阿比特龙抑制人 17,20-裂解酶和 17α-羟化酶,IC50 值分别为 27 和 30 nM[3]。阿比特龙的竞争性 Ki 值为 2.1 和 8.8 μM,可抑制重组人 3βHSD1 和 3βHSD2 的活性。在这两种细胞系中,10 μM 阿比特龙足以完全阻止 DHT 和 5α-二酮的合成。在强劲生长的部分中,abi 治疗显着减缓了 CRPC 的进展,在整个 4 周的治疗过程中有效地限制了肿瘤的生长 (P<0.00001)。阿比特龙抑制 LNCaP 中 Δ4-雄烯二酮 (AD) 的积累和 [3H]-脱氢表雄酮 (DHEA) 的消耗,IC50<1 μM[4]。
阿比特龙(Abiraterone) 抑制CYP17A1介导的雄激素合成。在富含CYP17A1的人肾上腺皮质微粒体中,1–100 nM的阿比特龙呈剂量依赖性降低: - 孕烯醇酮向17α-羟孕烯醇酮的转化(IC50=22 nM时降低约50%) [4] - 17α-羟孕烯醇酮向脱氢表雄酮(DHEA,C17,20-裂解酶产物)的转化(Ki=15 nM时降低约50%) [4] - 阿比特龙(Abiraterone) 抑制3β-HSD介导的类固醇转化。在表达3β-HSD的人肝微粒体中,0.5–10 μM的阿比特龙使孕烯醇酮向孕酮的转化降低:IC50=2.5 μM时降低约50%,10 μM时降低约90% [4] - 阿比特龙(Abiraterone) 抑制前列腺癌细胞增殖。用1–20 μM的阿比特龙处理LNCaP(雄激素敏感性)和C4-2(去势抵抗性前列腺癌,CRPC)细胞72小时: - MTT法显示LNCaP细胞活力降低:10 μM时降低约40%,20 μM时降低约65% [2] - Western blot显示AR靶基因表达降低:10 μM时C4-2细胞中前列腺特异性抗原(PSA)蛋白降低约55% [2] - 阿比特龙(Abiraterone) 不拮抗突变型AR。在过表达AR-V7的22Rv1细胞中,阿比特龙(最高20 μM)无法降低AR-V7介导的PSA表达,证实对截短型AR变体无活性 [2] |
| 体内研究 (In Vivo) |
先前已证明 0.5 mmol/kg/d 阿比特龙治疗剂量可产生 0.5 至 1 μM 之间的血清浓度。在对照组中,异种移植肿瘤的生长变化很大;只有一小部分肿瘤生长旺盛,而其他肿瘤则生长缓慢[4]。静脉内(5 mg/kg)给药后的分布容积(Vd)和清除率(Cl)分别测定为1.97 L/kg和31.2 mL/min/kg。确定2675ngh/mL是从时间零到无穷大时间点的血浆浓度-时间曲线下面积(AUC0-∞)。 0.73 小时是终末半衰期 (t1/2)。由于清除速度快,阿比特龙 (ART) 只能在静脉注射后两小时内进行定量[5]。
阿比特龙(Abiraterone) 抑制CRPC小鼠模型的肿瘤生长。携带C4-2异种移植瘤的去势雄性裸鼠,口服阿比特龙(50、100 mg/kg/天)或溶剂21天: - 肿瘤体积较溶剂组降低:50 mg/kg时降低约30%,100 mg/kg时降低约55%;肿瘤重量降低:50 mg/kg时降低约25%,100 mg/kg时降低约50% [3] - 血清睾酮水平(ELISA检测)从溶剂组的120±15 pg/mL降至100 mg/kg组的35±8 pg/mL [3] - 阿比特龙(Abiraterone) 在I期临床试验中显示疗效(人体体内数据)。47例CRPC患者口服阿比特龙 acetate(阿比特龙前药,50–2000 mg/天)联合泼尼松(5 mg,每日两次): - 76%的患者血清PSA降低≥50%;PSA进展中位时间为16周 [1] - 所有剂量≥250 mg/天的患者中,CYP17依赖的雄激素前体DHEA降低>90% [1] - 阿比特龙(Abiraterone) 在大鼠中表现出特定药代特征。雄性SD大鼠口服阿比特龙(10 mg/kg): - 血药浓度峰值(Cmax)为1.2±0.2 μg/mL,达峰时间(Tmax)为1.5±0.3小时;血药浓度-时间曲线下面积(AUC0-∞)为5.8±0.7 μg·h/mL [5] |
| 酶活实验 |
Enzyme assays/酶实验[4]
abiraterone作为抑制剂的孵育实验包含重组人3βHSD1或3βHSD2(在酵母微粒体中,每次孵育分别为3.2或25 μg蛋白),[3H]-孕烯醇酮(100,000 cpm, 1 - 20 μmol/L), abiraterone (5-20 μmol/L)或乙醇载体在0.2 ~ 1ml磷酸钾缓冲液中。37℃预孵育1 ~ 3分钟后,加入NAD+ (1 mmol/L), 37℃孵育15分钟。加入1 ~ 2ml乙酸乙酯:异辛烷(1:1)停止反应,提取类固醇到有机相。干燥后的提取物用薄层色谱(TLC)在塑料背衬硅胶板上用3:1氯仿:乙酸乙酯或高效液相色谱(HPLC)进行分离。对于薄层色谱,用碘蒸气鉴定含有类固醇的板的区域,用剪刀切除,并按所述用液体闪烁计数定量。HPLC法采用BioSafeII闪烁鸡尾酒法测定孕烯醇酮的放射性。以阿比特龙作为底物进行孵育,但以0.1 ~ 5 μmol/L未标记的阿比特龙代替孕烯醇酮,并采用HPLC定量转化。 配体结合试验[2] 将转染WT或T877A突变体AR或LNCaP细胞的PC-3细胞接种于24孔板中,在添加了css的无酚红培养基中培养24小时。为了确定[3H]-R1881与WT和T877A AR结合的动力学,将细胞用0.25-25nM [3H]-R1881处理2小时,然后洗涤、裂解并测量放射性。Kd和Bmax采用Graphpad Prism™软件非线性回归测定。当[3H]-R1881在WT和T877A AR突变体转染中达到几乎饱和AR所需的浓度(5nM)时,测定被试化合物对[3H]-R1881的置换。采用非线性回归法确定了[3H]-R1881置换50%时的浓度(EC50) CYP17A1(C17,20-裂解酶)活性实验: 1. 将人重组CYP17A1(昆虫细胞表达)与反应缓冲液(50 mM Tris-HCl pH 7.4、1 mM NADPH、10 μM细胞色素b5)及1 μM 17α-羟孕烯醇酮(底物)混合 [4] 2. 加入系列浓度的阿比特龙(Abiraterone)(0.1–100 nM),37°C孵育60分钟 [4] 3. 加入200 μL冰浴甲醇终止反应,通过高效液相色谱(HPLC,紫外检测波长240 nm)定量C17,20-裂解酶产物DHEA [4] 4. 计算相对于溶剂对照组的酶活性百分比,拟合竞争性抑制模型确定Ki值 [4] - 3β-HSD活性实验: 1. 将表达1型3β-HSD的人肝微粒体与反应缓冲液(50 mM Tris-HCl pH 7.5、1 mM NAD+、5 μM孕烯醇酮(底物))孵育 [4] 2. 加入阿比特龙(0.1–20 μM),37°C孵育30分钟 [4] 3. 加入100 μL乙腈终止反应,通过液相色谱-串联质谱(LC-MS/MS)定量3β-HSD产物孕酮 [4] 4. 对孕酮生成抑制率进行sigmoid剂量-反应拟合,计算IC50 [4] - 雄激素受体(AR)结合实验: 1. 将重组人野生型AR(或AR-V7突变体)固定于微孔板,加入0.5 nM [³H]-双氢睾酮(DHT,AR配体)和阿比特龙(0.1–100 μM) [2] 2. 25°C孵育120分钟,洗涤去除未结合的[³H]-DHT,通过液体闪烁计数法检测结合放射性 [2] 3. 采用Cheng-Prusoff方程计算Ki,未观察到显著结合(Ki>10 μM) [2] |
| 细胞实验 |
细胞生存能力[2]
LNCaP和VCaP细胞分别接种于96孔板中,在添加css的不含酚红或添加fbs的培养基中培养7 d。分别于24小时和96小时用化合物处理细胞,第7天通过添加CellTiter Glo和测量发光来测定细胞活力。 荧光素酶报告基因检测[2] 我们构建了一个PSA-ARE3-luc荧光素酶报告质粒,该质粒与人类AR表达质粒F527-AR(野生型(WT)或突变型)共转染;测序证实的突变)转化为PC-3细胞。将这些细胞播种在白色不透明的384孔板中,在添加10% css的不含酚红的RPMI 1640中生长30小时。然后用指定浓度的化合物和R1881处理细胞16小时。荧光素酶活性通过加入ONE Glo并在TopCount平板阅读器上测量发光来测定。转染效率和蛋白表达见补充图1。 C4-2 CRPC细胞增殖及AR靶基因实验: 1. C4-2细胞接种于96孔板(5×10³个/孔,活力实验)或6孔板(2×10⁵个/孔,Western blot),在含10%活性炭处理胎牛血清(去除雄激素)的RPMI 1640中培养 [2] 2. 用阿比特龙(Abiraterone)(1、5、10、20 μM)或溶剂(DMSO,终浓度<0.1%)处理细胞72小时 [2] 3. MTT实验:加入20 μL 5 mg/mL MTT孵育4小时,DMSO溶解甲瓒结晶,检测570 nm吸光度 [2] 4. Western blot:RIPA缓冲液裂解细胞,30 μg蛋白经SDS-PAGE分离后转移至PVDF膜,用抗PSA和抗β-肌动蛋白(内参)一抗孵育,化学发光法显影条带 [2] - LNCaP雄激素敏感性细胞实验: 1. LNCaP细胞接种于96孔板(4×10³个/孔),在含5%活性炭处理胎牛血清的无酚红DMEM中培养 [3] 2. 用阿比特龙(0.5–20 μM)预处理细胞2小时,再用1 nM睾酮刺激72小时 [3] 3. MTT法检测细胞活力;20 μM 阿比特龙 使睾酮诱导的增殖降低约65% [3] |
| 动物实验 |
溶于 0.3% 羟丙基纤维素;0.15 mmol/kg;皮下注射
LAPC-4 异种移植小鼠 小鼠异种移植研究[4] 使用 6 至 8 周龄的雄性 NOD/SCID 小鼠,所有研究均按照机构动物护理和使用委员会批准的方案进行。对小鼠进行手术去势,并植入 5 mg 90 天缓释 DHEA 颗粒,以模拟具有人类肾上腺生理功能的去势抵抗性前列腺癌 (CRPC)。两天后,将 7 × 10⁶ 个 LAPC4 细胞与 Matrigel 混合后皮下注射。每周测量肿瘤大小 2 至 3 次,肿瘤体积计算公式为:长 × 宽 × 高 × 0.52。当肿瘤体积达到 300 mm³ 时,将小鼠随机分配至载体组或阿比特龙治疗组。 阿比特龙组的小鼠接受 5 mL/kg 腹腔注射 0.5 mmol/kg/d(0.1 mL 5% 苯甲醇和 95% 红花油溶液),对照组小鼠仅接受载体注射,每天一次,每周 5 天,持续 4 周(每组 n = 8 只小鼠)。采用基于混合效应模型的方差分析(ANOVA)评估阿比特龙组和载体组之间的统计学显著性。 CRPC异种移植小鼠模型(C4-2细胞): 1. 将6-8周龄、20-25克的雄性裸鼠在皮下注射5×10⁶个C4-2细胞(悬浮于Matrigel中)前1周进行去势[3] 2. 当肿瘤体积达到100 mm³时,将小鼠随机分为3组(每组n=8):载体组(0.5%羧甲基纤维素[CMC]灌胃)、阿比特龙50 mg/kg/天组和阿比特龙100 mg/kg/天组[3] 3. 将阿比特龙溶解于0.5% CMC溶液中(超声处理使其溶解),每日一次灌胃给药。 21 天 [3] 4. 每 3 天测量一次肿瘤体积(体积 = 长度 × 宽度² / 2);研究结束时,处死小鼠,切除肿瘤并称重,收集血清,通过 ELISA 检测睾酮 [3] - 大鼠药代动力学研究: 1. 雄性 Sprague-Dawley 大鼠(250–300 g)在给药前禁食 12 小时,可自由饮水 [5] 2. 将阿比特龙溶解于甲醇中(10 mg/mL 储备液),然后用生理盐水稀释至 1 mg/mL(最终甲醇浓度 <5%)。大鼠经口灌胃给予阿比特龙(10 mg/kg,10 mL/kg 体积)[5] 3. 分别于给药后 0.25、0.5、1、1.5、2、4、6、8、12 和 24 小时从颈静脉采集血样(0.2 mL)。通过离心(3000 × g,10 分钟,4°C)分离血浆,并储存于 -80°C [5] 4. 采用经验证的 RP-HPLC/UV 法(检测波长 248 nm)测定血浆中阿比特龙的浓度;通过非房室模型分析计算药代动力学参数 [5] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在隔夜空腹的健康受试者中,单次服用 500 mg 醋酸阿比特龙后,几何平均值(± 标准差)Cmax 为 73 (± 44) ng/mL,AUC0-∞ 为 373 (± 249) ng·hr/mL。单次服用 125 mg 至 625 mg 醋酸阿比特龙均观察到剂量比例关系。一组转移性去势抵抗性前列腺癌 (mCRPC) 患者每日服用 1000 mg:稳态时,平均(± 标准差)Cmax 为 226 (± 178) ng/mL,AUC 为 993 (± 639) ng·hr/mL。转移性去势抵抗性前列腺癌患者口服醋酸阿比特龙后,中位 Tmax 为 2 小时。在体内,醋酸阿比特龙会转化为阿比特龙。在其他醋酸阿比特龙制剂的临床研究中,超过99%的分析样本中,醋酸阿比特龙的血浆浓度低于检测限(< 0.2 ng/mL)。与食物同服时,醋酸阿比特龙的全身暴露量会增加。在健康受试者中,与隔夜空腹相比,单次服用500 mg醋酸阿比特龙后,若同时摄入高脂餐(56-60%脂肪,900-1000卡路里),则阿比特龙的Cmax值大约高出6.5倍,AUC0-∞值大约高出4.4倍。鉴于膳食成分和组成存在正常差异,与食物同服阿比特龙可能导致药物暴露量增加且波动较大。 口服14C-醋酸阿比特龙后,约88%的放射性剂量从粪便中排出:粪便中的主要化合物是未代谢的醋酸阿比特龙和阿比特龙,分别约占给药剂量的55%和22%。约5%的剂量从尿液中排出。 平均(±标准差)表观稳态分布容积为19,669(±13,358)升。 代谢/代谢物 醋酸阿比特龙转化为活性代谢物阿比特龙的过程可能由酯酶介导,但尚未鉴定出具体的酯酶。在人体血浆中,两种主要的循环代谢物是硫酸阿比特龙(由 CYP3A4 和 SULT2A1 生成)和 N-氧化硫酸阿比特龙(由 SULT2A1 生成)。这两种代谢物各占阿比特龙暴露量的约 43%,且无药理活性。 阿比特龙已知的人体代谢物包括硫酸阿比特龙。 生物半衰期 在转移性去势抵抗性前列腺癌 (mCRPC) 患者中,阿比特龙在血浆中的平均(± 标准差)末端半衰期为 12(± 5)小时。 口服吸收: - 在大鼠中:阿比特龙的口服生物利用度约为 36 ± 5%(与静脉注射 5 mg/kg 相比)。口服10 mg/kg剂量后,Cmax = 1.2 ± 0.2 μg/mL,Tmax = 1.5 ± 0.3 小时 [5] - 在人体中:醋酸阿比特龙(前药)口服吸收;口服1000 mg后,阿比特龙(活性形式)在Tmax = 2 ± 0.5 小时时达到Cmax = 0.8 ± 0.2 μg/mL。食物可使Cmax增加约10倍,因此需空腹给药 [1, 3] - 分布: - 在大鼠中:分布容积 (Vd) = 12 ± 2 L/kg,表明其组织渗透广泛。阿比特龙在肾上腺和前列腺中蓄积(组织/血浆比为8-10倍)[5] - 在人体中:Vd = 19 ± 4 L/kg;血浆蛋白结合率 = 99.6 ± 0.2%(与白蛋白和α1-酸性糖蛋白结合)[1, 3] - 代谢: - 阿比特龙主要在肝脏通过CYP3A4和SULT2A1代谢。主要代谢物无活性(例如,N-氧化物、硫酸盐结合物);未检测到活性代谢物[3, 5] - 排泄: - 在大鼠中:70 ± 6%的阿比特龙在72小时内经粪便排泄(65%为代谢物,5%为原药),15 ± 3%经尿液排泄(全部为代谢物)[5] - 在人体中:消除半衰期 (t1/2) = 12 ± 2 小时;80%经粪便排泄,10%经尿液排泄[1, 3] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
接受阿比特龙治疗的患者中,高达 13% 会出现血清转氨酶升高,而接受安慰剂或对照药物治疗的患者中,这一比例为 1% 至 8%,但这些异常通常是轻微的、短暂的,并且不伴有症状或黄疸。接受阿比特龙治疗的患者中,ALT 升高超过正常值上限 (ULN) 5 倍的比例为 6%。 可能性评分:C(可能是临床上明显的肝损伤的罕见原因)。 蛋白结合 阿比特龙与人血浆蛋白(白蛋白和 α-1 酸性糖蛋白)的结合率很高 (>99%)。 人体不良反应(I 期试验): - 最常见的副作用(每日 1000 mg 阿比特龙 + 泼尼松):体液潴留 (36%)、高血压 (28%)、低钾血症 (21%) 和疲劳 (19%)。这些症状归因于盐皮质激素水平升高(由于 CYP17 抑制),并可被泼尼松缓解 [1] - 剂量 ≤1000 mg/天时未观察到严重的肝毒性(ALT/AST > 正常上限的 5 倍)[1] - 动物毒性: - 在大鼠中:急性口服 LD50 > 2000 mg/kg。一项为期 28 天的重复给药研究(50、200、500 mg/kg/天)显示,肝肾功能(ALT、AST、BUN、肌酐)或器官重量均无变化[5] - 在犬类中:连续 14 天口服 100 mg/kg/天会导致轻度肾上腺萎缩(停药后可逆)[3] - 药物相互作用: - 阿比特龙是 CYP3A4 的底物:与酮康唑(CYP3A4 抑制剂)合用可使阿比特龙的 AUC 增加约 4 倍;与利福平(CYP3A4 诱导剂)合用可使 AUC 降低约 70%[3] |
| 参考文献 |
|
| 其他信息 |
药效学
在体内,醋酸阿比特龙迅速水解为阿比特龙,后者发挥其药理作用。阿比特龙可降低血清睾酮和其他雄激素水平。可能会观察到血清前列腺特异性抗原 (PSA) 水平的变化。 作用机制:阿比特龙通过阻断两种关键酶来抑制雄激素合成: - CYP17A1:阻止肾上腺、睾丸和前列腺肿瘤组织中孕烯醇酮/孕酮转化为雄激素前体(DHEA、雄烯二酮)[1, 3] - 3β-HSD:阻断孕烯醇酮转化为孕酮(盐皮质激素/雄激素的前体),进一步抑制类固醇生成[4] - 它不直接与雄激素受体 (AR) 结合,这使其区别于抗雄激素(例如 MDV3100)[2] - 治疗适应症:阿比特龙(以醋酸阿比特龙的形式)已获准用于治疗转移性去势抵抗性前列腺癌 (mCRPC)。它与泼尼松联合使用,以对抗盐皮质激素过多症[1, 3] - 临床原理:去势抵抗性前列腺癌(CRPC)即使经过去势治疗(血清睾酮水平低下)后,仍受激素驱动,因为肿瘤会在局部合成雄激素。阿比特龙可抑制这种局部合成,从而降低PSA水平并使肿瘤消退[1, 3] - 耐药机制:耐药性的出现与雄激素受体(AR)突变(例如AR-V7)或类固醇生成酶(例如3β-HSD)表达增加有关,因此需要增加阿比特龙剂量或与AR拮抗剂(例如MDV3100)联合使用[2, 4] - 前药说明:醋酸阿比特龙是一种前药,可在体内水解为阿比特龙(活性形式)。醋酸酯部分可提高口服吸收率和稳定性[1, 3] |
| 分子式 |
C24H31NO
|
|---|---|
| 分子量 |
349.51
|
| 精确质量 |
349.24
|
| 元素分析 |
C, 82.47; H, 8.94; N, 4.01; O, 4.58
|
| CAS号 |
154229-19-3
|
| 相关CAS号 |
Abiraterone acetate;154229-18-2;Abiraterone-d4;2122245-62-7
|
| PubChem CID |
132971
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.14g/cm3
|
| 沸点 |
500.2±50.0 °C at 760 mmHg
|
| 熔点 |
227-228 °C
|
| 闪点 |
256.3±30.1 °C
|
| 蒸汽压 |
0.0±1.3 mmHg at 25°C
|
| 折射率 |
1.606
|
| LogP |
5.7
|
| tPSA |
33.12
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
26
|
| 分子复杂度/Complexity |
636
|
| 定义原子立体中心数目 |
6
|
| SMILES |
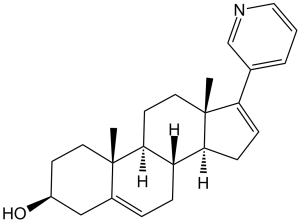
C[C@]12CC[C@@H](CC1=CC[C@@H]3[C@@H]2CC[C@]4([C@H]3CC=C4C5=CN=CC=C5)C)O
|
| InChi Key |
GZOSMCIZMLWJML-VJLLXTKPSA-N
|
| InChi Code |
InChI=1S/C24H31NO/c1-23-11-9-18(26)14-17(23)5-6-19-21-8-7-20(16-4-3-13-25-15-16)24(21,2)12-10-22(19)23/h3-5,7,13,15,18-19,21-22,26H,6,8-12,14H2,1-2H3/t18-,19-,21-,22-,23-,24+/m0/s1
|
| 化学名 |
(3S,8R,9S,10R,13S,14S)-10,13-dimethyl-17-(pyridin-3-yl)-2,3,4,7,8,9,10,11,12,13,14,15-dodecahydro-1H-cyclopenta[a]phenanthren-3-ol.
|
| 别名 |
Abiraterone; CB 7598; CB7598; CB-7598; 17-(3-Pyridyl)androsta-5,16-dien-3beta-ol; (3beta)-17-(3-pyridinyl)-androsta-5,16-dien-3-ol; Abiraterone (CB-7598); US trade name: Zytiga.
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.8611 mL | 14.3057 mL | 28.6115 mL | |
| 5 mM | 0.5722 mL | 2.8611 mL | 5.7223 mL | |
| 10 mM | 0.2861 mL | 1.4306 mL | 2.8611 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03348670 | Active, not recruiting | Drug: Abiraterone - Usual Drug: Abiraterone - Study |
Prostate Cancer | Han Xu, M.D., Ph.D., FAPCR, Sponsor-Investigator, IRB Chair |
August 18, 2023 | Phase 2 Phase 3 |
| NCT05968599 | Active, not recruiting | Drug: Enzalutamide Drug: Abiraterone acetate |
Prostatic Neoplasms, Castration-Resistant |
Pfizer | July 24, 2023 | |
| NCT05520138 | Completed | Drug: Enzalutamide Drug: Abiraterone acetate |
Prostatic Neoplasms, Castration-Resistant |
Pfizer | August 29, 2022 | |
| NCT03565835 | Active, not recruiting | Drug: Abiraterone Acetate Drug: Prednisone |
Prostatic Neoplasms | Montefiore Medical Center | June 13, 2018 | Phase 2 |
|
|
|