| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
GSK-3β (IC50 = 6.7 nM); GSK-3α (IC50 = 10 nM); cdc2 (IC50 = 8800 nM)
|
|||
|---|---|---|---|---|
| 体外研究 (In Vitro) |
与其最接近的同源物 CDC2 和 ERK2 以及其他蛋白激酶相比,CHIR-99021 对 GSK-3 的选择性高出 500 倍以上。 CHIR-99021 仅对 23 种非激酶具有适度的抑制作用,并且与 22 种具有药理学意义的受体仅具有微弱的结合。在表达胰岛素受体的 CHO-IR 细胞中,CHIR-99021 会激活糖原合酶 (GS),EC50 为 0.763 μM[1]。
|
|||
| 体内研究 (In Vivo) |
在 2 型糖尿病啮齿动物模型中,口服 30 mg/kg CHIR-99021 可改善葡萄糖代谢。口服给药后三到四个小时,血浆葡萄糖最大程度降低(大约 150 mg/dl),血浆胰岛素水平保持在或低于控制水平。在 ZDF 大鼠中,在口服葡萄糖挑战前每小时口服 16 或 48 mg/kg 剂量的 CHIR-99021 可显着改善葡萄糖耐量,在 16 mg/kg 和 48 mg/kg 剂量下血浆葡萄糖水平分别下降 14% 和 33%分别为 mg/kg 剂量。较高剂量的 CHIR-99021 还可减轻口服葡萄糖激发前的高血糖[1]。
|
|||
| 酶活实验 |
所有激酶测定都遵循相同的核心方案,肽底物和激活剂浓度变化如下所述。聚丙烯96孔板填充300μl/孔缓冲液(50 mmol/l三HCl、10 mmol/l MgCl2、1 mmol/l EGTA、1 mmol/1二硫苏糖醇、25 mmol/lβ-甘油磷酸、1 mmol/l NaF、0.01%BSA、pH 7.5),其中含有激酶、肽底物和任何激活剂。这些测定的激酶浓度、肽底物和激活剂(如适用)信息如下:GSK-3α(27 nmol/l和0.5μmol/l生物素CREB肽);GSK-3β(29 nmol/l,和0.5μmol/l生物素CREB肽);cdc2(0.8 nmol/l和0.5μmol/l生物素组蛋白H1肽);erk2(400单位/ml和髓鞘碱性蛋白包被的闪光板[Perkin-Elmer]);PKC-α(1.6 nmol/l,0.5μmol/l生物素组蛋白H1肽和0.1 mg/ml磷脂酰丝氨酸+0.01 mg/ml甘油二酯);PKC-ζ(0.1 nmol/l,0.5μmol/l生物素-PKC-86肽和50μg/ml磷脂酰丝氨酸+5μg/ml二酰甘油);akt1(5.55nmol/l和0.5μmol/l生物素磷酸化AKT肽);p70 S6激酶(1.5 nmol/l和0.5μmol/l生物素GGGKRRRLASLRA);p90 RSK2(0.049单位/ml和0.5μmol/l生物素GGGKRRRLASLRA);c-src(4.1单位/ml和0.5μmol/l生物素KVEKIGEGTYGVVYK);Tie2(1μg/ml和200 nmol/l生物素GGGGAPEDL-YKDFLT);flt1(1.8 nmol/l和0.25μmol/l KDRY1175[B91616]生物素GGGGQDGKDYIVLPI-NH2);KDR(0.95 nmol/l和0.25μmol/l KDRY1175[B91616]生物素-GGGQDGKDYIVLPI-NH2);bFGF受体酪氨酸激酶(RTK;2 nmol/l和0.25μmol/l KDRY1175[B91616]生物素-GGGGGQDGKDYIVLPI-NH2);IGF1 RTK(1.91 nmol/l和1μmol/l生物素GGGGKKKSPGEYVNIEFG酰胺);胰岛素RTK(使用DG44 IR细胞);AMP激酶(470单位/ml、50μmol/l SAMS肽和300μmol/l AMP);pdk1(0.25 nmol/l、2.9 nmol/l未活化的Akt和20μmol/l DOPC和DOPS+2μmol/l PIP3);CHK1(1.4 nmol/l和0.5μmol/l生物素-cdc25肽);CK1-ε(3 nmol/l,和0.2μmol/l生物素肽);DNA PK;和磷脂酰肌醇(PI)3-激酶(5nmol/l和2μg/ml PI)。在所有无细胞测定中,将受试化合物或对照加入3.5μl DMSO中,然后加入50μl ATP储备,以产生1μmol/l ATP的最终浓度。孵育后,将一式三份的100μl等分试样转移到含有100μl/孔50μmol/l ATP和20 mmol/l EDTA的Combiplate八板(LabSystems,赫尔辛基,芬兰)中。1小时后,用PBS冲洗孔5次,填充200μl闪烁液,密封,静置30分钟,并在闪烁计数器中计数。所有步骤均在室温下进行。抑制计算为100%×(抑制−无酶对照)/(DMSO对照−无酶控制)。[1]
|
|||
| 细胞实验 |
表达人胰岛素受体的 CHO-IR 细胞在含有 10% 胎牛血清且不含次黄嘌呤的 Hamm's F12 培养基中生长至 80% 汇合。在 2 ml 不含胎牛血清的培养基中,将胰蛋白酶处理的细胞以每孔 1×106 个细胞的密度接种到 6 孔板中。 24 小时后,将培养基更换为 1 ml 含有 GSK-3 抑制剂或对照(DMSO 最终浓度 <0.1%)的无血清培养基,37°C 培养 30 分钟。裂解细胞并离心 15 分钟。 4°C/14000g。使用 Thomas 等人开发的滤纸测定法,将 GS 活性比计算为存在和不存在 5 mmol/l 6-磷酸葡萄糖时 GS 活性之间的差异。
|
|||
| 动物实验 |
|
|||
| 参考文献 |
[1]. Diabetes. 2003 Mar;52(3):588-95.
[2]. PLoS One.2013;8(3):e58501.
|
|||
| 其他信息 |
胰岛素抵抗在2型糖尿病的发生发展中起着核心作用,但胰岛素作用的具体缺陷仍有待阐明。糖原合成酶激酶3 (GSK-3) 可负调控胰岛素信号传导的多个方面,已有研究报道糖尿病啮齿动物和人类骨骼肌中GSK-3水平升高。目前关于高选择性GSK-3抑制剂在胰岛素抵抗条件下调节胰岛素作用的研究信息有限。本研究描述了一类新型取代氨基嘧啶衍生物,该衍生物能高效抑制人GSK-3(Ki < 10 nmol/L),且对其他20种蛋白激酶的选择性至少高500倍。这些低分子量化合物在转染胰岛素受体的培养CHO细胞和从Sprague-Dawley大鼠分离的原代肝细胞中,以约100 nmol/L的浓度即可激活糖原合成酶;在瘦型Zucker大鼠和ZDF大鼠分离的I型骨骼肌中,以500 nmol/L的浓度即可激活糖原合成酶。有趣的是,这些GSK-3抑制剂增强了胰岛素抵抗型ZDF大鼠I型骨骼肌中胰岛素刺激的葡萄糖转运,但对胰岛素敏感型Zucker瘦型大鼠则无此作用。单次口服或皮下注射这些抑制剂(30-48 mg/kg)可迅速降低ZDF大鼠和db/db小鼠在口服或静脉注射葡萄糖负荷后的血糖水平,并改善葡萄糖利用,且不会引起低血糖或显著升高胰岛素水平。总的来说,我们的研究结果表明,这些选择性GSK-3抑制剂可能作为急性起效的治疗药物,用于治疗2型糖尿病的胰岛素抵抗。[1]
我们已鉴定出Wnt10b是脂肪生成的重要抑制剂,必须抑制Wnt10b才能使前脂肪细胞在体外分化。在此,我们证明糖原合成酶激酶3的特异性抑制剂CHIR 99021能够模拟前脂肪细胞中的Wnt信号通路。CHIR 99021能够稳定胞质游离的β-catenin,并通过阻断CCAAT/增强子结合蛋白α和过氧化物酶体增殖物激活受体γ的诱导来抑制脂肪生成。在脂肪生成的最初3天内,当3T3-L1细胞暴露于CHIR 99021的任何24小时时间段内,前脂肪细胞的分化都会受到抑制。与此抑制时间框架一致,Wnt10b mRNA 的表达在分化诱导后受到抑制,6 小时后下降 50%,36 小时后完全抑制。在用于诱导分化的试剂中,将 3T3-L1 细胞暴露于甲基异丁基黄嘌呤或 cAMP 足以抑制 Wnt10b mRNA 的表达。Wnt10b 对脂肪生成的抑制作用可能由 Wnt 受体 Frizzled 1、2 和/或 5 以及辅助受体低密度脂蛋白受体相关蛋白 5 和 6 介导。这些受体与 Wnt10b 一样,在脂肪前体细胞和基质血管细胞中高表达。最后,我们证明,通过表达分泌的 Frizzled 相关蛋白来破坏细胞外 Wnt 信号传导会导致脂肪细胞自发转化。[2] 最近的研究进展表明,糖尿病患者 β 细胞功能和数量的再生是可能的。针对目前无法提供最佳血糖控制的糖尿病疗法,再生疗法可能是一种替代治疗选择。本文报道,小分子抑制剂或RNA干扰可抑制GSK3的活性,从而刺激INS-1E大鼠胰岛瘤细胞的复制。特异性强效的GSK3抑制剂还能减轻高浓度葡萄糖和饱和脂肪酸棕榈酸酯对INS-1E细胞的毒性作用。此外,用结构多样的小分子GSK3抑制剂处理分离的大鼠胰岛,可使β细胞的复制速率较对照组提高2-3倍。我们认为GSK3是β细胞复制和存活的调节因子。此外,我们的研究结果表明,特异性GSK3抑制剂可能在β细胞再生疗法中具有实际应用价值。[3] |
| 分子式 |
C22H20CL4N8
|
|---|---|
| 分子量 |
538.26
|
| 精确质量 |
538.053
|
| 元素分析 |
C, 49.09; H, 3.75; Cl, 26.34; N, 20.82
|
| CAS号 |
2109414-84-6
|
| 相关CAS号 |
252917-06-9;1782235-14-6 (3HCl);2109414-84-6 (2HCl);1797989-42-4 (HCl);
|
| PubChem CID |
91826519
|
| 外观&性状 |
Solid powder
|
| tPSA |
115
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
34
|
| 分子复杂度/Complexity |
645
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
OOMHEMQQCHEWDS-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C22H18Cl2N8.2ClH/c1-13-10-29-21(31-13)17-12-30-22(32-20(17)16-4-3-15(23)8-18(16)24)27-7-6-26-19-5-2-14(9-25)11-28-19;;/h2-5,8,10-12H,6-7H2,1H3,(H,26,28)(H,29,31)(H,27,30,32);2*1H
|
| 化学名 |
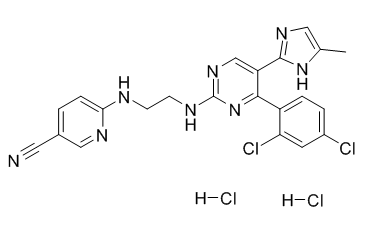
6-((2-((4-(2,4-dichlorophenyl)-5-(5-methyl-1H-imidazol-2-yl)pyrimidin-2-yl)amino)ethyl)amino)nicotinonitrile dihydrochloride
|
| 别名 |
2109414-84-6; UNII-X6BE5J2G31; Laduviglusib dihydrochloride; CHIR-99021 dihydrochloride; CHIR-911 dihydrochloride;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
Typically soluble in DMSO (e.g. > 10 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8578 mL | 9.2892 mL | 18.5784 mL | |
| 5 mM | 0.3716 mL | 1.8578 mL | 3.7157 mL | |
| 10 mM | 0.1858 mL | 0.9289 mL | 1.8578 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Status | Interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03616223 | Completed | Drug: FX-322 Drug: Placebo |
Sensorineural Hearing Loss |
Frequency Therapeutics | July 3, 2018 | Phase 1 Phase 2 |